Упорные золотомышьяковые руды в нашей стране перерабатываются в ограниченной количестве из-за отсутствия рациональной и экологобезопасной технологии. В Забайкалье имеются большие запасы руд, содержащих тонкое и дисперсное золото. Золото в этих рудах находится в тесной ассоциации с арсенопиритом, входя в структуру в виде тонковкрапленных или эмульсионных ассоциаций. Данные руды представляют собой крупный сырьевой источник получения золота.
В золотосодержащих рудах мышьяк, в основном, представлен в виде арсенопирита и частично арсенатов кальция и железа и накапливается в хвостохранилищах и отвалах обогатительных фабрик. Существует точка зрения, что мышьяк в хвостохранилищах золотоизвлекательных фабрик находится в устойчивой форме арсенопирита, скородита и в экологическом плане безопасен. Однако это справедливо, когда эти соединения находятся в массиве пород в условиях равновесного состояния. Как показала многолетняя практика, арсенопирит, скородит и другие малорастворимые в воде соединения мышьяка, находясь в хвостохранилищах и отвалах в тонкодисперсной форме в смеси с солями, реагентами обогатительных фабрик и в условиях подвижности кислотно-щелочного и кислородного баланса среды, претерпевают окисление, растворяются в фильтрующихся водах и загрязняют окружающую среду. Так, например, наличие в отвалах карбонатов, гидроксида кальция способствует раскислению арсенопирита и вымыванию мышьяка фильтрующими водами [1].
При пирометаллургическом технологическом переделе мышьяк переходит практически во все твердые продукты обжига, а также концентрируется в отходящих газах и сточных водах. Поэтому проблема вывода мышьяка, значительно усложняющего технологию извлечения металлов, ухудшающего качество товарной продукции и загрязняющего окружающую среду, является актуальной задачей.
Из отходов мышьяка в естественных условиях устойчивы и могут складироваться без захоронения арсениды железа, скородит и сульфиды мышьяка. Последние являются наиболее концентрированными по содержанию основного компонента и компактны по объему. Они относятся к IV классу опасности [2].
При переработке традиционными гидрометаллургическими способами руд (и концентратов) данного типа не удается достигнуть высокой степени извлечения золота (< 60¸70 %).
Анализ существующих технологий, использующих обжиг при переработке руд данного типа показывает, что они страдают существенными недостатками: сложное технологическое оборудование; использование в качестве сульфидизатора чистого пирита, дорогостоящей элементарной серы и необходимость дополнительного процесса доокисления остаточной серы на выходе огарка из печи; недостаточное вскрытие арсенопирита и выделение из него мелкого и тонкого золота и неполное удаление мышьяка. Получаемые отвальные материалы, содержат арсенаты кальция и железа, которые при хранении растворяются и загрязняют окружающую среду.
Поэтому требуется усовершенствование процесса обжига для создания рациональной технологии переработки данного сырья, которая бы позволила решить и экологический вопрос – перевести мышьяк в малотоксичную сульфидную форму.
Одним из путей создания рациональной технологии переработки данного сырья является обжиг арсенопирита в атмосфере перегретого водяного пара с пиритом.
В основу обжига заложен процесс взаимодействия пирита и пирротина с парами воды. Данные исследования показали, что первичной стадией взаимодействия является термическая диссоциация пирита, продукты которой взаимодействуют с парами воды. Диссоциация пирита на пирротин сопровождается выделением элементарной серы. В связи с тем, что процесс взаимодействия сульфида металла с водяным паром протекает при повышенных температурах, механизм парооксидирования был выявлен с учетом термической диссоциации сульфидов. Разрыв химических связей между атомами серы и металла сопровождается либо газообразной, либо конденсатной диссоциацией. Диссоциация сульфидов может происходить по реакции:
MeSm ↔MeSm–n+Sn (1)
Если диссоциация сульфида металла происходит по реакции (1), то в газовой фазе следует ожидать присутствие H2S, SO2 и Н2, так как будет протекать реакция между элементарной серой и водяным паром. Водород же является продуктом окисления металла (например, Fe до FeO) или его оксида (например, FeO до Fe3O4) водяным паром. При диссоциации исходный сульфид металла переходит в более бедные по сере соединения, что предопределяет возможность дальнейшей диссоциации по маршруту реакции (1). В результате происходит образование металла, т.е. суммарно-начальный процесс оксидирования сульфида металла может быть записан следующим образом:
2MeS2 + 2m ∙ H2O ↔ m ∙ SO2 + m ∙ H2S + m ∙ H2 +2Me. (2)
Образовавшийся металл взаимодействует с парами воды с образованием оксида, а диоксид серы с водородом с образованием сероводорода. Таким образом, при взаимодействии пирита с водой при высоких температурах в системе могут присутствовать пары элементарной серы, сернистое железо, сероводород и водород.
Если в систему FeS2–H2O внести арсенопирит, то произойдет образование сульфидов мышьяка [3]
2FeAsS + 4FeS2 + 12H2O → 2Fe3O4 + As2S3 + 4H2S + 3SO2 + 8H2 .
Таким образом, обжиг в атмосфере водяного пара позволяет перевести мышьяк в малотоксичную сульфидную форму и утилизировать его с минимальным отрицательным воздействием на окружающую среду. Процесс сопровождается декрипитацией минералов, что значительно улучшает дальнейшее выделение золота.
Объектом для исследований явилась проба золотосодержащего арсенопиритного концентрата (Забайкальский край). Рудными минералами являются арсенопирит (преимущественно) и пирит. В данной пробе содержится – золота 44,5 г/т и серебра 26,2 г/т.
В выбранных расчетным путем оптимальных условиях обжига (температура в печи 700-750 оС, соотношение концентрат : сульфидизатор равно 3:1, продолжительность обжига 20 мин.) были проведены лабораторные опыты. Обжиг целесообразно вести при температуре 700-730 оС (увеличение температуры до 750 оС повышает инкапсуляцию золота в огарке). Степень деарсенизации составляет 99,7-99,9 %, а степень десульфидизации 97-98 %. Высокая степень десульфидизации исходного сырья снимает необходимость доокисления остаточной серы. Конечной железосодержащей фазой в огарке является магнетит (Fe3O4).
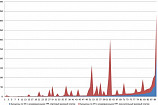
Исследования по цианированию полученного огарка показали, что растворение золота протекает с высокой скоростью и практически заканчивается в течение первого часа выщелачивания (рис. 1.). Степень извлечения золота из концентрата и огарка составляет 57 % и 94 % соответственно. Повышение извлечения составляет почти 50 % по сравнению с необожженной пробой. Степень извлечения серебра составляет порядка 92 % [4].

Рис. 1. Выщелачивание золота цианистым раствором: а) для класса крупности –0,5+0,25; б) для класса флотационной крупности (70 % класса –0,074 мм)
На основании проведенных исследований предложена принципиальная технологическая схема переработки труднообогатимого золотосодержащего арсенопиритного концентрата (рис. 2.). Золотосодержащая арсенопиритная руда или концентрат направляется на дробление и последующее стадиальное измельчение с выделением класса –0,5 мм, которые смешиваются с пиритным концентратом и направляется на обжиг в атмосфере перегретого водяного пара при температуре 730 оС при соотношении арсенопиритная руда (концентрат) : пиритный концентрат, равным 3:1. Подачу смеси осуществляли со скоростью, обеспечивающей время обжига не менее 20 мин [5].
При обжиге сульфиды железа окисляются до магнетита, мышьяк возгоняется в виде сульфида As2S3 и конденсируется в твердую фазу с парами воды. Полученный огарок направляется на дальнейшее обогащение на концентрационном столе с целью выделения крупного золота. Степень извлечения крупного золота составила 22,19 %. Далее хвосты гравитационного обогащения подвергаются магнитной сепарации для извлечения железа в магнетитовый концентрат. Результаты разделения продуктов следующие: магнитная фракция – 50 %, немагнитная фракция – 50 %. Введение двух перечисток в процессе магнитной сепарации обеспечивает получение магнетитового концентрата с извлечением в него железа 90,47 %.

Рис. 2. Технологическая схема переработки золотосодержащих арсенопиритных руд и концентратов
Немагнитная фракция направляется на дальнейшую переработку для извлечения золота по традиционной технологической схеме переработки (цианированием).
Газы и пыль из печи подаются на циклоны. При охлаждении газов происходит конденсация дисульфида мышьяка. Полученный сульфид мышьяка направляют на захоронение или дальнейшую переработку. Вода находится в обороте.
Таким образом, обжиг золотосодержащей арсенопиритной руды с сульфидизатором в паровой атмосфере позволяет, наряду с повышением извлечения золота, снизить экологическую нагрузку на окружающую природную среду за счет перевода мышьяка в малотоксичную сульфидную форму и дополнительно выделить магнетитовый концентрат.
Список литературы:
- Новин А.П. Пути повышения извлечения золота из руд и песков / А.П. Новин, Ю.В. Румянцев, О.Г. Перфильев // Сб. науч. трудов ин-та Иргиредмет. – Иркутск, 1981.
- Исабаев С.М. Сульфидирование мышьяксодержащих соединений и разработка способов вывода мышьяка из концентратов и промпродуктов цветной металлургии: автореф. дисс. … д-ра техн. наук. – Иркутск, 1991. – 39 с.
- Гуляшинов А.Н., Антропова И.Г., Палеев П.Л., Мязин В.П., Гуляшинов П.А. Водяной пар в комбинированных схемах переработки полиметаллических руд // Сб. Материалов IX Конгресса обогатителей стран СНГ. – М.: МИСиС, 2013. – Т.1. – С. 203-206.
- Палеев П.Л., Гуляшинов А.Н., Хантургаева Г.И., Мязин В.П. Деарсенизация золотосодержащих арсенопиритных руд // Горный информационно-аналитический бюллетень (ГИАБ). Серия Забайкалье. М.: Издательство «Горная книга», 2009. – С. 181-185.
- Патент № 2309187 РФ. Способ переработки золотосодержащих арсенопиритных руд и концентратов // Палеев П.Л., Гуляшинов А.Н., Антропова И.Г., Хантургаева Г.И. Опубликован 27.10.2007. Бюлл. № 30.
Палеев П.Л., Гуляшинов А.Н., Антропова И.Г., Гуляшинов П.А. – Федеральное государственное бюджетное учреждение науки Байкальский институт природопользования Сибирского отделения РАН (БИП СО РАН) г. Улан-Удэ, Россия.
Опубликовано в журнале “Золото и технологии” № 2(20)/июнь 2013 г.